FDA twierdzi, że leki na ciśnienie krwi przypominało o obawy dotyczące ryzyka raka

Prawie połowa ciebie.S. Dorośli mają nadciśnienie, częściej określane jako wysokie ciśnienie krwi, zgodnie z Centers for Disease Control and Prevention (CDC). Większość z tych pacjentów zaleca się przyjmowanie leków, które mogą kontrolować ciśnienie krwi i zapobiegać poważniejszymi powikłaniami, takimi jak choroby serca i udar. Jeśli jednak jesteś jednym z wielu Amerykanów przyjmujących te leki codziennie, będziesz chciał być świadomy najnowszego wycofania, które wpływa na jeden leki na ciśnienie krwi, które mogłyby wyrządzić więcej szkody niż pożytku, zgodnie z U.S. Food and Drug Administration (FDA). Czytaj dalej, aby dowiedzieć się, co zalecają eksperci, jeśli masz tę receptę.
Przeczytaj następny: Wysokie ciśnienie krwi? Picie 2 filiżanek kawy codziennie podwójnie choroby serca ryzyko śmierci, nowe badanie stwierdza.
„Nieczystość” została wykryta, gdy Quinapril przeszedł testowanie.

W grudniu. 21, FDA ogłosiło, że Lupine Pharmaceuticals dobrowolnie przywołuje cztery wiele tabletek chinapril, które były dystrybuowane dla pacjentów. Leki to enzym konwertujący angiotensynę (ACE), który obniża ciśnienie krwi u pacjentów z nadciśnieniem. AE0FCC31AE342FD3A1346EBBB1F342FCB
Zgodnie z zawiadomieniem FDA ostatnie testy wykazały „obecność zanieczyszczenia nitrozaminy”, zwaną N-nitrozo-kwinapryl, który był powyżej akceptowalnego poziomu dziennego przyjmowania (ADI). Dotknięte działki obejmują zarówno tabletki z Quinapril 20 mg, jak i 40-mg tabletki Quinapril USP, które zostały dystrybuowane w 90 butelkach do „hurtowników, łańcuchów narkotykowych, apteków wysyłkowych i supermarketów."
Wiadomość pojawia się po Aurobindo Pharma USA, Inc. Dobrowolnie przywołał dwie wiele tabletek Quinapril i hydrochlorotiazyd.
Notozaminy są w rzeczywistości powszechne i nie zawsze powodują niepokój.
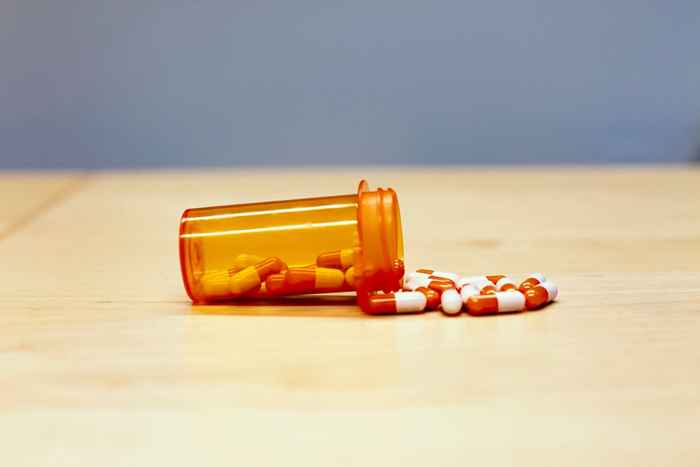
FDA wyjaśnia, że nitrozoaminy nie zawsze jest niebezpieczne-każdy jest narażony na pewien poziom tych związków, ponieważ są one powszechnie spotykane w „Wodzie i żywności, w tym wyleczone i grillowane mięso, produkty mleczne i warzywa i warzywa.„Ale kiedy ludzie są narażeni na wyższy poziom nitrozamin w dłuższym czasie, ryzyko raka może wzrosnąć.
FDA ma całą stronę, która zawiera przegląd zanieczyszczeń nitrozaminy w różnych lekach. Według strony FDA aktywnie bada obecność tych zanieczyszczeń i zaleca, aby producenci przypominali leki, które mogą znajdować się powyżej uznanych na granicy limitów ADI.
Agencja wyjaśnia, że jeśli twoje leki mają poziomy nitrozaminy w granicach ADI lub poniżej, i bierzesz go codziennie przez 70 lat, nie oczekujesz zwiększonego ryzyka raka. Ryzyko jest związane wyłącznie z tymi, którzy przyjmują wyższe poziomy przez dłuższy czas.
Do tej pory Lupine nie otrzymał żadnych raportów o chorobie związanych z tabletkami Quinapril.
Powiązane: Aby uzyskać więcej aktualnych informacji, zapisz się do naszego codziennego biuletynu.
Możesz sprawdzić leki, aby sprawdzić, czy jest to część wycofania.

Wszystkie cztery wiele przywołanych tabletek Quinapril zostały rozpowszechnione między 15 marca 2021 r. A września. 1, 2022, gdy Lupine zaprzestał marketingu leku we wrześniu tego roku. Pojedyncza partia wycofanych 20 mg tabletek ma datę ważności kwietnia 2023 r., Liczbę G102929, krajowy kodeks narkotykowy (NDC) 68180-558-09 (90.) oraz uniwersalny kod produktu 368180558095.
Pozostałe trzy partie zawierają 40 mg tabletek z NDC 68180-554-09 (90-tych) i UPC 368180554097. Pierwsze dwa partie G100533 i G100534-Both mają datę ważności w grudniu. 2022 i ostatni LOT-G203071-HAS Data ważności marca 2023.
UPC znajdują się w skanonalnym kodzie kreskowym, a NDC są wymienione nad marką na opakowaniu. Numery partii są wydrukowane z boku etykiety butelki.
Skontaktuj się z lekarzem, jeśli weźmiesz tabletki Quinapril.

Według FDA Lupine nazywa obecnie wszystkich podmiotów, w których leki były dystrybuowane w celu poinformowania ich o wycofaniu się i zorganizowaniu zwrotu dotkniętych produktów. W międzyczasie osoby z lekiem w magazynie są proszone o natychmiastowe zaprzestanie dystrybucji z wycofanych działek.
Konsumenci, którzy przyjmują tabletki Quinapril o 20 mg lub 40 mg, zaleca się skontaktowanie. W międzyczasie kontynuuj przyjmowanie leków zgodnie z zaleceniami, mówi FDA.
Jeśli masz pytania dotyczące wycofania, możesz skontaktować się z Inmar Rx Solutions, Inc. o (877) 538-8445, od poniedziałku do piątku między 9 a.M. i 5 p.M. Wschodni czas standardowy (EST). Jeśli doświadczasz reakcji niepożądanej lub napotkasz problem jakości związany z używaniem Quinapril, FDA prosi o zgłoszenie go do programu raportowania zdarzeń niepożądanych MedWatch. Możesz to zrobić online lub za pośrednictwem zwykłej poczty lub faksu.
Best Life oferuje najbardziej aktualne informacje od najlepszych ekspertów, nowych badań i agencji zdrowotnych, ale nasze treści nie mają zastąpić profesjonalnych wskazówek. Jeśli chodzi o leki, które przyjmujesz lub inne pytania zdrowotne, zawsze skonsultuj się z lekarzem bezpośrednio.


